近日,兩篇發(fā)表在國(guó)際雜志Nature Immunology和Journal of Clinical Investigation上的研究報(bào)告中,來(lái)自La Jolla免疫研究所等機(jī)構(gòu)的科學(xué)家們有望利用輔助T細(xì)胞來(lái)幫助治療人類機(jī)體的腫瘤。如今,研究人員正在尋找一組稱之為“新抗原”(neoantigens)的獨(dú)特突變,其能讓機(jī)體免疫系統(tǒng)有效區(qū)分腫瘤細(xì)胞和正常細(xì)胞,研究人員旨在幫助宿主機(jī)體的免疫系統(tǒng)對(duì)新抗原產(chǎn)生反應(yīng)并靶向摧毀腫瘤細(xì)胞。
如今這一領(lǐng)域的研究已經(jīng)促使科學(xué)家們開(kāi)發(fā)出了挽救生命的抗體療法,比如免疫檢查點(diǎn)抑制劑,其依賴于抗體來(lái)幫助免疫細(xì)胞殺滅腫瘤,但不幸的是,基于抗體的癌癥免疫療法并不是對(duì)所有患者都有效。于是研究人員就一直在尋找抗體之外的東西,他們深入研究了免疫系統(tǒng)CD4+輔助T細(xì)胞是如何幫助檢測(cè)新抗原的。文章中,研究者Schoenberger及其同時(shí)揭示了如何利用CD4+ T細(xì)胞同時(shí)還增強(qiáng)CD8+ 殺傷性T細(xì)胞的抗癌潛能;事實(shí)上,研究人員展示了一種新型的疫苗設(shè)計(jì)策略,其能招募兩種類型的T細(xì)胞來(lái)破壞較大的腫瘤。Schoenberger表示,治療性癌癥疫苗能發(fā)揮一定的作用,但它們應(yīng)該利用CD4+ T細(xì)胞和CD8+ T細(xì)胞的自然協(xié)同作用。
正如研究人員指出的那樣,CD4+ T細(xì)胞和CD8+ T細(xì)胞在抵御病毒和細(xì)菌時(shí)已經(jīng)能協(xié)同發(fā)揮作用了,那么為何不能學(xué)習(xí)免疫系統(tǒng)保護(hù)我們的自然方式,并將其轉(zhuǎn)化為抵御癌癥的策略呢?發(fā)表在Nature Immunology雜志上的研究報(bào)告中,研究人員闡明了CD4+ T細(xì)胞在識(shí)別腫瘤細(xì)胞上的必要角色,這一策略依賴于一種創(chuàng)新性的方法來(lái)預(yù)測(cè)哪種腫瘤新抗原會(huì)誘發(fā)強(qiáng)大的CD4+ T細(xì)胞反應(yīng)。
正如研究人員解釋的那樣,腫瘤細(xì)胞起源于機(jī)體的正常細(xì)胞,這意味著機(jī)體很難識(shí)別識(shí)別腫瘤細(xì)胞是危險(xiǎn)的,而諸如病毒等其它威脅往往也會(huì)攜帶非常不像人類的肽類序列,在CD4+ T細(xì)胞的刺激下,稱之為樹(shù)突狀細(xì)胞的免疫細(xì)胞就能捕獲這些肽類序列,并將其展示給CD8+ T細(xì)胞,從而促使免疫系統(tǒng)進(jìn)入紅色警報(bào)狀態(tài),CD8+ T細(xì)胞能殺死腫瘤,但其需要與CD4+ T細(xì)胞協(xié)同作用才能有效完成這一任務(wù)。但腫瘤細(xì)胞與正常細(xì)胞之間共享著大多數(shù)肽類序列,因此免疫系統(tǒng)很難看到,為了解決這個(gè)問(wèn)題,研究人員設(shè)計(jì)了一種計(jì)算工具來(lái)識(shí)別遺傳突變和能作為新抗原的特殊肽類,從而就能有效區(qū)分腫瘤細(xì)胞和其鄰近細(xì)胞了。
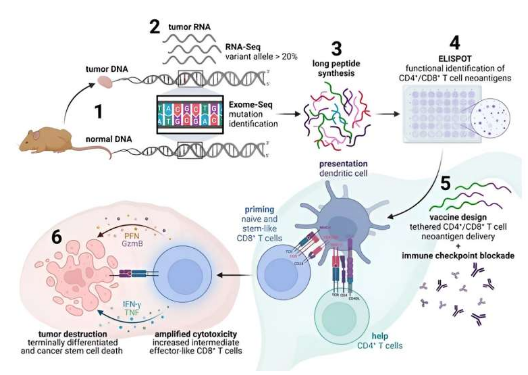
科學(xué)家有望利用輔助性T細(xì)胞來(lái)幫助治療人類癌癥。
圖片來(lái)源:Journal of Clinical Investigation (2023). DOI:10.1172/JCI164258
發(fā)表在Nature Immunology雜志上的研究表明,能識(shí)別單一靶向突變的CD4+ T細(xì)胞通常會(huì)驅(qū)動(dòng)一種多樣化的CD8+ T細(xì)胞反應(yīng),從而清除較大的腫瘤,于是研究人員測(cè)試了能識(shí)別這些靶向突變親和力的T細(xì)胞,即抗原受體與新抗原結(jié)合的強(qiáng)度到底有多大,研究結(jié)果表明,新抗原特異性的CD4+ T細(xì)胞能介導(dǎo)其在一系列親和力上的作用。研究者Schoenberger說(shuō)道,這是一項(xiàng)全新的發(fā)現(xiàn),因?yàn)椴](méi)有人在T細(xì)胞受體水平上研究過(guò)新抗原特異性的CD4+細(xì)胞庫(kù)。研究者還發(fā)現(xiàn),當(dāng)轉(zhuǎn)移性的CD4+ T細(xì)胞被誘導(dǎo)發(fā)育成干細(xì)胞記憶樣CD4+ T細(xì)胞時(shí),最有效的反應(yīng)就會(huì)發(fā)生,這種類型的T細(xì)胞就會(huì)被賦予長(zhǎng)壽和產(chǎn)生強(qiáng)大效應(yīng)細(xì)胞的能力,隨著相關(guān)研究從實(shí)驗(yàn)室走向臨床,這些研究發(fā)現(xiàn)也會(huì)在不久的未來(lái)轉(zhuǎn)化為臨床試驗(yàn)。
在第二項(xiàng)發(fā)表在Journal of Clinical Investigation雜志上的研究報(bào)告中,研究人員揭示了一種新型疫苗策略是如何誘導(dǎo)CD4+ T細(xì)胞和CD8+ T細(xì)胞相互協(xié)作來(lái)摧毀小鼠模型機(jī)體中的大型侵襲性腫瘤的。研究人員從一組侵襲性的鱗狀細(xì)胞癌開(kāi)始研究,其包含少量的突變,就好像人類癌癥一樣;研究人員識(shí)別出了270個(gè)突變,其能使這些腫瘤從正常細(xì)胞中脫穎而出,同時(shí)研究人員對(duì)其中39個(gè)突變進(jìn)行了深入研究。最后他們將范圍縮小到五種突變,其能被天然抗腫瘤的T細(xì)胞反應(yīng)所識(shí)別,其中一些突變能被CD4+ T細(xì)胞所靶向作用,而另一些則被CD8+ T細(xì)胞所靶向作用;值得注意的是,只有CD4+ T細(xì)胞和CD8+ T細(xì)胞靶向作用的突變能誘發(fā)機(jī)體抵御腫瘤的保護(hù)性或治療性反應(yīng)。
最后研究者表示,這些新抗原必須在物理上與介導(dǎo)療法相關(guān)聯(lián),只要疫苗能通過(guò)相同的抗原呈遞細(xì)胞來(lái)激活CD4+ T細(xì)胞和CD8+ T細(xì)胞,我們就能促使大的腫瘤消失;展望未來(lái),研究人員計(jì)劃通過(guò)聯(lián)合研究來(lái)分析是否這種類型的關(guān)聯(lián)疫苗在人類患者中有效,他們希望未來(lái)的臨床試驗(yàn)或能給患者尤其是侵襲性腫瘤患者的治療帶來(lái)希望。如果研究人員能將檢查點(diǎn)阻滯療法與個(gè)體化癌癥疫苗相結(jié)合起來(lái),那么或許就能大大增加因免疫檢查點(diǎn)阻滯療法獲益的患者數(shù)量。




 17312606166
17312606166