上海交通大學(xué)醫(yī)學(xué)院藥理學(xué)和化學(xué)生物學(xué)系高小玲課題組設(shè)計并率先構(gòu)建了仿生脂蛋白納米藥物,可用于降低腦內(nèi)β淀粉樣蛋白沉積、延緩阿爾茨海默病的疾病進程。該雜志同時刊登了國際知名納米醫(yī)學(xué)專家、以色列特拉維夫大學(xué)Dan Peer教授專門為此撰寫的述評文章,指出這種精妙設(shè)計的結(jié)構(gòu)有望為阿爾茲海默病的治療干預(yù)提供一種全新的納米藥物。相關(guān)文章發(fā)表于近期的《ACS Nano》雜志上。"
阿爾茨海默病是一種最為常見的老年性癡呆類型,但目前臨床上尚缺乏有效的干預(yù)手段。業(yè)已證明阿爾茨海默病的核心致病物質(zhì)是β淀粉樣蛋白,通過降低腦內(nèi)β淀粉樣蛋白水平,早期干預(yù)阿爾茨海默病的病理生理進程已成為國際生物醫(yī)藥界共同探索的領(lǐng)域。
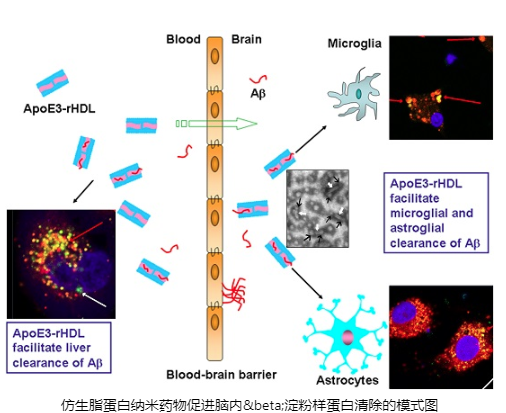
高小玲課題組長期從事腦靶向納米遞藥系統(tǒng)和針對阿爾茨海默病診療的關(guān)鍵納米技術(shù)研究。最新研究成功模擬天然高密度脂蛋白,設(shè)計并率先構(gòu)建了既能通過血腦屏障又具有β淀粉樣蛋白親和特性的仿生脂蛋白納米藥物,通過介導(dǎo)腦內(nèi)小膠質(zhì)細胞、星形膠質(zhì)細胞和外周肝細胞對β淀粉樣蛋白的攝取和降解,有效促進了腦內(nèi)β淀粉樣蛋白的清除。
科研人員介紹,為保護中樞穩(wěn)定性,人體的腦血管內(nèi)皮細胞間緊密連接形成血腦屏障,如同一道閘門,98%以上的小分子藥物和100%的大分子藥物不能進入大腦發(fā)生作用,而該仿生納米藥物模擬了人體內(nèi)的高密度脂蛋白,可順利通過血腦屏障,作用于大腦。實驗證明,該仿生納米藥物的應(yīng)用大大改善了阿爾茨海默病疾病模型小鼠的認知功能。同時該納米藥物可高效載藥,特別適于針對阿爾茨海默病的長期多模式治療,具有良好的轉(zhuǎn)化應(yīng)用前景。
上述研究成果引起了國外學(xué)者的關(guān)注,除Dan Peer教授作出述評外,美國化學(xué)會周刊Chemical & Engineering News在該文章在線發(fā)表后第一時間發(fā)表題為“Lipoprotein Nanoparticles Boost Memory In mice With Alzheimer’s(Nanomedicine: Particles that resemble high-density lipoprotein clear out clumps of amyloid-β)”的圖文報道。長期從事脂蛋白研究的專家、北德克薩斯大學(xué)健康科學(xué)中心Andras G. Lacko教授認為這是一個縝密精巧的概念驗證研究,提供了一種阿爾茨海默病治療的新策略。
該論文的第一作者為碩士研究生宋清香。此項成果得到上海交通大學(xué)醫(yī)學(xué)院陳紅專教授和加拿大多倫多大學(xué)鄭崗教授的共同指導(dǎo),并受到國家重大科學(xué)研究計劃、國家自然科學(xué)基金和上海市科委國際合作等基金資助。科研人員表示今后將在藥物作用方式、載藥特性等方面做進一步研究,目前該成果已申請國家發(fā)明專利,并正在申請國際專利。




 17312606166
17312606166